PRACTICA EXTRACCIÓN Y SEPARACIÓN DE DNA
ANTECEDENTES
Además del agua, los carbohidratos, las proteínas y los lípidos, los seres vivos están constituidos por otras moléculas que, aunque en menor cantidad, desempeñan funciones muy importantes.
Los ácidos nucleícos (DNA y RNA) son biomoléculas solubles en agua que desempeñan funciones diversas. Son moléculas complejas producidas por las células vivas; son esenciales para todos los organismos vivo. Estas moléculas gobiernan el desarrollo del cuerpo y sus características específicas, ya que proporcionan la información hereditaria y ponen en funcionamiento la producción de proteínas.
OBJETIVÓ
Extraer DNA y rna de tejidos animales o vegetales e identificarlos como tales.
MATERIAL
1.-T ubos de centrifuga 1ml
2.-Tubos de ensayo de 5ml
3.-Centrifuga
4.-Micropipetas de 1000 y 200 ul
5.-Agua destilada estéril (20 ml para todos)
6.-Etanol al 100% frio (20 ml es suficiente)
7.-NaCL 3M
8.-Buffer de extracción de ADN (Urea, NaCl, EDTA, 20 ml es suficiente para todos)
9.-Fenol/cloroformo/isoprapol frio (20 ml es suficiente para todos)
10.-Mortero y pistilo
11.-Aguacate, cacahuate, hojas, carne, hígado, sangre.
12.-Papel aluminio
13.-Cleenpack
14.-Guantes
PROCEDIMIENTO
A) Rompimiento de membranas y paredes celulares.
Toma una muestra de tejido (5 gr. Aprox.) que hayas elegido y homogeneízalo, es decir muélelo con el mortero, si el tejido es muy duro licúalo en seco.
Coloca tu muestra molida (1 gr. Aprox.) en un tubo de eppendorf de 1 ml y agrégale el Buffer de extracción (tris-HCL 0.005 M, EDTA 0.02 M, NaCl 0.35 M, Urea 7 M) a temperatura de cuarto (500 ul Aprox.).
Cuando hayas agregado el Buffer de extracción a tu muestra, agítala e incúbala por 10 minutos con agitación esporádica.
C) Separación de Proteinas, Carbohidratos y Lípidos.
A la mezcla que tienes en un tubo de ensayo agrégale 500 ul. De Fenol/cloroformo/isopropanol frio usa guantes y no inhales los vapores.
Agita vigorosamente en Vortex, cuidando que no se tire el contenido del tubo, deja reposar a temperatura ambiente por 5 minutos.
Extrae la fase acuosa (500 ul Aprox.) con una micropipeta. Si no se separan las fases centrifuga a 3000 rpm por 10 min. Ten cuidado de equilibrar la centrifuga.
Extrae la fase acuosa superior una vez centrifugada.
CONCLUSIÓN
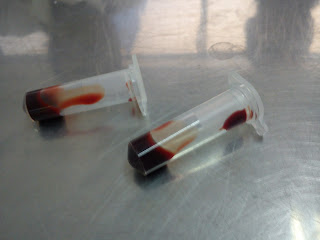
El resultado de esta indagación se obtuvo mediante esta prueba de extracción de hígado de pollo y sangre de humano, se pudo observar la diferenciación que existe entre el DNA del higado y la sangre , la cual en esta muestra se identifico la fase que hay entre los carbohidratos, lípidos y proteínas las cuales mediante los tubos de ensayo pude prestar atención a cerca de la diferencia que se obtenía de esta espécimen del ADN, los cuales hubo separación de las proteínas y separación de lípidos así como la apartamiento de carbohidratos. Este modelo se logró obtener mediante una centrifuga la cual contenía diferentes tipos de reactivos los cuales dieron resultados diferentes, que se pudieron distinguir en clases con las demás muestras de los demás compañeros del equipo en el que algunos solamente pudieron adquirir proteínas, lípidos e viceversa ya que en algunas muestras eran desiguales a los de los demás equipos por que eran diferentes tejidos.
Para alcanzar este resultado se realizo en un material de”DAIGGER” Vortex Genie 2, en el que se pusieron las muestras para ser disueltas por este equipo, después se pudo llevar al proceso de centrifugación en el que hubo separación de las proteínas, como lípidos y carbohidratos.
1.-Investiga por que el DNA en solución se precipita en presencia de un alcohol frio.
El DNA y ortos componentes celulares, como lípidos, azucares y proteínas, se disuelven en una solución de lisis. El AND tiene carga negativa debido a los grupos fosfato de su estructura, y esta carga eléctrica es lo que hace soluble a esta molécula. Cuando se añada sal al a muestra, los iones sodio con carga positiva son atraídos por las cargas negativas de ADN, neutralizando la carga del ADN. Esto permite a las moléculas de ADN unirse en vez de repelerse entre sí. La adición de alcohol frio precipita el ADN dado que es insoluble en altas concentraciones de sal y alcohol. El ADN precipitado forma unas finas hebras blancas y visibles en el límite de separación de la fase de alcohol mientras que el resto de las sustancias permanecen disueltas.
2.-Como separamos e nuestra muestra el DNA del RNA.
Si en nuestra muestra necesitamos uno de los dos modelos le ponemos una enzima que ayude a degradar a la otra (DNAsas o RNAsas), para prepararos se puede utilizar dos tipos de métodos los cuales se pueden manejar:
1.- centrifugación en gradiente de cloruro de cesio (separa por densidad).
2.- cromatografía de exclusión molecular (poseen distintos tamaños).
Sé que existen más métodos que se podrán utilizar pero como referencia madamas podremos utilizar uno de estos dos.
3.-¿Cuál es la función del cloroformo?
Como ya saben el cloroformo de formula molecular CHCI₃ es un compuesto químico que es usado como reactivo relajante por lípidos orgánicos, este reactivo es usado para dormir a personas con periodos muy cortos. Es comúnmente utilizado en el área de biología molecular para varios procesos, como l extracción de ADN delisados celulares.
4.-¿Cómo podrías cuantificar la cantidad de ADN de tu muestra?
La cuantificación es un sitio donde se valora la calidad de ADN y cantidad de ADN obtenido durante el proceso de extracción y purificación del ADN.
Se llevaría el proceso en el área de cuantificación: solo después de que el ADN de la muestra ha sido aislado, la cantidad y calidad podrá determinarse con precisión. La determinación de la cantidad de ADN en una muestra es esencial para la mayoría de los ensayos basados en PCR, ya que concentraciones de ADN relativamente bajas permite que se desarrolle mejor la amplificación de los sitios de interés. La cuantificación del ADN de muestra de referencia (sangra) se realiza mediante un equipo Nanodrop marca Thermo y para la cuantificación del ADN extraído de muestras forenses como tejido muscular, huesos, tejidos embebidos en parafina, células espermáticas en caso de violoaci0on, etc.
Es utilizada un técnica más sensible como en la que se desarrolla en el pcr Tiempo Readl marca Applied Biosystems, permitiendo conocer la concentración del ADN que se obtuvo posteriormente al proceso de extracción, es un ensayo que monitores el producto de PCR mientras tiene lugar la amplificación, analiza ciclo a ciclo los cambios en la señal de florescencia generados durante las tres fases de la PCR.
5.- ¿Cuál es la función y la importancia del ADN en los organismos?
El ADN es el que contiene el mensaje genético para toda la función y organización celular. Es, en definitivo, la molécula que controla todos los procesos vitales para los seres vivos, además de ser el principal constituyente de los cromosomas celulares. Es el material genético de todos los organismos celulares y casi todos los virus. Llaqué el ADN se encarga de llevar la información necesaria para dirigir la síntesis de proteínas y la replicación. Se concreta como síntesis de proteína a la producción de las proteínas que necesita la célula o el virus para realizar su actividad y desarrollarse.la replicación como sabemos es el conjunto de reacciones por medio de los cuales el ADN se copia así mismo cada vez que una célula o un virus se reproduce y se transmite a la descendencia la información que contiene. En casi todos los organismos celulares el ADN esta organizado en forma e cromosomas, situados en el núcleo de la célula.